|
ΑΝΑΣΚΟΠΗΣΗ (REVIEW) Βιβλιογραφική
αναφορά (Citation)
|
|
IDEA Medical Newsletter 202311:22,1. Available at https://www.idea-lab.gr/newslet20231102201.htm
|
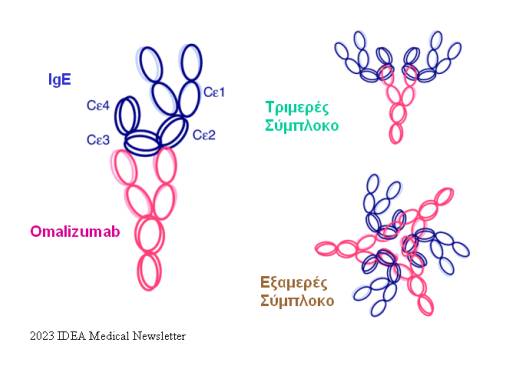
ΕΙΚΟΝΑ 1. H ομαλιζουμάμπη είναι εξανθρωποποιημένο IgG1 μονοκλωνικό αντίσωμα, που συνδέεται με την IgE στην
περιοχή Cε3. Η ομαλιζουμάμπη σχηματίζει
τριμερή και εξαμερή σύμπλοκα με την IgE, τα οποία
κυκλοφορούν στο αίμα. Έτσι τα επίπεδα ολικής IgE φαίνεται
να αυξάνονται μετά από την έναρξη θεραπείας με ομαλιζουμάμπη
(Tong και
Wesemann).
-----
Αναφυλαξία και άλλες
παρενέργειες από ομαλιζουμάμπηΑνοσολογία
της σαρκοείδωσης
Αντώνιοης Παπακωνσταντίνου
-----
Περίληψη
Η
ομαλιζουμάμπη είναι μονοκλωνικό αντι-IgE αντίσωμα, που χρησιμοποιείται
για τη θεραπεία του αλλεργικού άσθματος και της χρόνιας κνίδωσης. Στην ανασκόπηση αυτή αναφερόμαστε στις ανεπιθύμητες
ενέργειες του φαρμάκου με έμφαση στην αναφυλαξία που αποτελεί κατάσταση απειλητική για τη ζωή. Οι υπόλοιπες παρενέργειες της ομαλιζουμάμπης περιλαμβάνουν πιθανό
κίνδυνο εμφάνισης κακοήθειας,
κίνδυνο παρασιτικής νόσου και ανοσολογικές αντιδράσεις όπως
ορονοσία και σύνδρομο Churg-Strauss.σαρκοείδωση είναι
πολυσυστηματική φλεγμονώδης νόσος, που χαρακτηρίζεται από σχηματισμό
----- κοκκιωμάτων χωρίς κεντρική
τυροειδοποίηση. Η νόσος προσβάλλει
συχνότερα τους πνεύμονες, τους λεμφαδένες, τους οφθαλμούς και το δέρμα. Στα ιδιαίτερα ανοσολογικά χαρακτηριστικά
της νόσου περιλαμβάνεται η έντονη πόλωση στην παραγωγή κυτταροκινών των Th1 κυττάρων και TNF στα σημεία της φλεγμονής. Αντίθετα είναι μειωμένες οι κυτταροκίνες
που απελευθερώνονται από τα Th2 κύτταρα. Ο ρόλος των Treg κυττάρων καθώς και των
μηχανισμών της συμφυούς ανοσίας παραμένει αβέβαιος. Τέλος
μεγαλύτερες προσπάθειες πρέπει να καταβληθούν προκειμένου να διευκρινιστούν
οι μηχανισμοί ίνωσης στη σαρκοείδωση.
Εισαγωγή
Η Η ομαλιζουμάμπη (omalizumab) είναι ένα ανασυνδυασμένο εξανθρωποποιημένο μονοκλωνικό
αντίσωμα IgG1 έναντι της ανθρώπινης ανοσοσφαιρίνης Ε (IgE) (Tong και Wesemann). Έτσι αποτρέπει την
αλληλεπίδρασή της με τον υποδοχέα υψηλής συγγένειας Fc-ε-RI που
απαντάται τυπικά σε ηωσινόφιλα, σιτευτικά κύτταρα (mast cells) και
βασεόφιλα και παίζει κρίσιμο ρόλο στη μεταβολική διαδικασία
των αλλεργιών. Η
ομαλιζουμάμπη έχει χρησιμοποιηθεί με επιτυχία στην αντιμετώπιση του μέτριου
έως σοβαρού άσθματος που προκαλείται από IgE και, πιο πρόσφατα, έχει
χρησιμοποιηθεί στη χρόνια κνίδωση (Kumar και Zito, 2022).σαρκοείδωση είναι πολυσυστηματική
φλεγμονώδης νόσος που χαρακτηρίζεται από το σχηματισμό κοκκιωμάτων (φυμάτια)
χωρίς τη χαρακτηριστική κεντρική νέκρωση της φυματίωσης
(τυροειδοποίηση). Η νόσος προσβάλλει
συχνότερα τους πνεύμονες, τους ενδοθωρακικούς λεμφαδένες, τους οφθαλμούς και το δέρμα
-----.
Ανεπιθύμητες ενέργειες της
ομαλιζουμάμπηςοσοπαθολογία
Ο σχηματισμός
κοκκιωμάτων αρχίζει από τα φαγοκύτταρα της συμφυούς ανοσολογικής απόκρισης
που εκφράζουν υποδοχείς αναγνώρισης προτύπου, όπως είναι οι υποδοχείς δίκην toll (TLR).. Τα
φαγοκύτταρα προσπαθούν να ενσωματώσουν το υποκινητικό παθογόνο και να προετοιμάσουν τo προσαρμοζόμενo ανοσοποιητικό
σύστημα παρουσιάζοντας τα ξένα αντιγόνα στην επιφάνεια των MHC μορίων τάξης Ι ή ΙΙ. Ανάλογα με το παθογόνο αίτιο και διάφορους γενετικούς παράγοντες και
επιγενετικούς παράγοντες η επικρατούσα προσαρμοζόμενη άνοση αντίδραση είναι Th1 είτε Th2 είτε Th17, ανάλογα με τον τύπο των Τ κυττάρων που
ενεργοποιούνται. Όταν
επικρατεί η ενεργοποίηση των Th1 κυττάρων αναφερόμαστε σε Th1 άνοση απόκριση (εδώ
βιβλιογραφία από ιδεα μεδικαλ νιουσλεττερ). Η επακόλουθη απελευθέρωση προφλεγμονωδών
κυτταροκινών από τα κύτταρα της συμφυούς και της προσαρμοζόμενης ανοσίας κατευθύνει το
σχηματισμό κοκκιωμάτων.
Στη
σαρκοείδωση τα κοκκιώματα αποτελούνται από επιθηλιοειδή κύτταρα, μονοπύρηνα
και CD4+ Τ κύτταρα
με λίγα περιφερικά CD8+ Τ
κύτταρα. Το ποσοστό των Τ
λεμφοκυττάρων στο βρογχοκυψελιδικό έκπλυμα (BAL) είναι αυξημένο και τυπικά αποτελεί το 20-60%
του Η ομαλιζουμάμπη γενικάσυ
χαρακτηρίζεται από καλό προφίλ ασφάλειας.
Οι
κύριες ανεπιθύμητες ενέργειες που αναφέρθηκαν σε κλινικές
δοκιμές ήταν αντιδράσεις στο σημείο της ένεσης (45%), ιογενής λοίμωξη (23%),
λοίμωξη του ανώτερου αναπνευστικού συστήματος (20%), ιγμορίτιδα (16%),
κεφαλαλγία (15%) και φαρυγγίτιδα (11%) (Kumar και Zito, 2022).
Υπάρχουν
αναφορές για αναφυλακτικές αντιδράσεις που εμφανίστηκαν με την ομαλιζουμάμπη, συνήθως
εντός 2 ωρών από την πρώτη ή τις επόμενες δόσεις, αν και η συχνότητα
εμφάνισης είναι χαμηλή (0,1 έως 0,2%). Αξίζει να
σημειωθεί ότι ως σήμερα οι αναφορές έχουν γίνει μόνο σε ασθενείς
με άσθμα και όχι σε πάσχοντες από χρόνια
κνίδωση (Plosker και Keam, 2008). Λόγω της σοβαρότητας
των αναφυλακτικών αντιδράσεων συστήθηκε από 2 επιστημονικά αμερικανικά ιδρύματα
ανοσολογίας – αλλεργίας Κοινή Ομάδα Εργασίας (Joint Task
Force) για την ομαλιζουμάμπη. Η Ομάδα διαπίστωσε ότι από τους
39510 ασθενείς που έλαβαν το φάρμακο από τον Ιούνιο του 2003 έως και τον
Δεκέμβριο του 2005, 35 ασθενείς παρουσίασαν 41 επεισόδια αναφυλαξίας, που
αντιστοιχούν σε ποσοστό 0,09%. Συστήθηκε όλοι οι ασθενείς να παρακολουθούνται
από γιατρό επί 2ωρο, τουλάχιστον για τις τρεις πρώτες
ενέσεις.
Συστήθηκε επίσης στους θεραπευόμενους να χορηγηθεί
προληπτικά συσκευή αυτοχορήγησης αδρεναλίνης (Cox L et al, 2007).
Στη
βιβλιογραφία έχει αναφερθεί κίνδυνος κακοήθειας που σχετίζεται με την IgE. Μια συγκεντρωτική ανάλυση (pooled analysis) των κλινικών
δοκιμών φάσης 1 έως 4 το 2012 έδειξε ότι δεν υπήρχε σαφής συσχέτιση μεταξύ
της θεραπείας με ομαλιζουμάμπη και του κινδύνου κακοήθειας σε τυχαιοποιημένες,
διπλά τυφλές, ελεγχόμενες με εικονικό φάρμακο μελέτες (Busse W et al, 2012).
Η
ανοσοσφαιρίνη Ε θεωρείται ως το κύριο
αντίσωμα για την καταπολέμηση των παρασιτικών νοσημάτων. Υπάρχουν ενδείξεις ότι σε
περιοχές όπου ενδημούν λοιμώξεις από έλμινθες, η θεραπεία
με ομαλιζουμάμπη αυξάνει ελαφρώς τον κίνδυνο νόσησης του ασθενούς
σε σύγκριση με το εικονικό φάρμακο (Kumar και Zito, 2022).
Περιπτώσεις ορονοσίας
ή/και αγγειίτιδας Churg-Strauss μετά από θεραπεία με
ομαλιζουμάμπη αναφέρονται στη βιβλιογραφία. Ωστόσο,
εξακολουθεί να είναι αβέβαιο εάν υπάρχει αιτιολογική συσχέτιση μεταξύ της
θεραπείας με ομαλιζουμάμπη και του Churg-Strauss. Συγκεκριμένα δεν είναι
σαφές εάν το σύνδρομο αποτελεί παρενέργεια ή πρόκειται για προϋπάρχουσα
κατάσταση που προηγουμένως είχε καλυφθεί λόγω των
μακροχρονίων θεραπειών με κορτικοστεροειδή τα οποία γενικά λαμβάνουν
αυτοί οι ασθενείς (Kumar και Zito, 2022).
Τέλος έχουν
αναφερθεί δύο περιστατικά παροδικής αλωπεκίας σε ασθενείς
με χρόνια κνίδωση που έλαβαν θεραπεία με ομαλιζουμάμπη (Kumar και Zito, 2022).
-----νολικού αριθμού κυττάρων. Επικρατούν τα CD4+ κύτταρα και ο λόγος CD4+:CD8+ κυττάρων που φυσιολογικά είναι 2:1 σε ασθενείς με σαρκοείδωση ανέρχεται σε > 3:1.
Th1 πόλωση
Είναι πλέον
τεκμηριωμένο ότι η
κοκκιωματώδης φλεγμονή της σαρκοείδωσης συνδέεται με μεγάλη παραγωγή
κυτταροκινών που συνοδεύουν την Th1 άνοση απόκριση (Th1 πόλωση). Η έκκριση IL-12, IL-18 και IL-27 που ενισχύουν την Th1 απόκριση είναι αυξημένη. Ιδιαίτερα αυξημένη είναι η έκκριση
ιντερφερόνης-γ (IFN-γ) που είναι η χαρακτηριστική κυτταροκίνη που
εκκρίνεται από τα βοηθητικά Τ κύτταρα τύπου 1. Η IFN-γ ενεργοποιεί τα μακροφάγα και δρα συνεργικά με
άλλες κυτταροκίνες (όπως ο TNF) στη θανάτωση των μικροβίων. Οι
ιντερλευκίνες IL-2 και IL-15, που επίσης υπερεκκρίνονται στη σαρκοείδωση
ενισχύουν τον κυτταρικό πολλαπλασιασμό των Τ κυττάρων και ελαττώνουν το ρυθμό
απόπτωσης (προγραμματισμένος κυτταρικός θάνατος) τους. Τα CD8+ T κύτταρα που εκφράζουν την IFN-γ συμβάλλουν στη Th1 πόλωση που παρατηρειται στη σαρκοείδωση. Στα ίδια
πλαίσια στους πάσχοντες εμφανίζεται αυξημένη παραγωγή του μεταγραφικού
παράγοντα STAT1, που ρυθμίζει τη διαφοροποίηση των Th1 κυττάρων. (Όταν μπεί η
βιβλιογραφία να αλλαχθεί η σειρά αυτών των ιντερλευκινών για να μη μοιάζει με
το αρχικό κείμενο).
Αντίθετα οι
ιντερλευκίνες IL-4 και IL-5 των Th2 κυττάρων υποεκκρίνονται. Ομοίως υποεκκρίνονται στον τόπο της
φλεγμονής οι περισσότερες χημειοκίνες και οι υποδοχείς χημειοκινών που
σχετίζονται με την Th2 άνοση απόκριση. Εξαίρεση, τουλάχιστον για μια υποομάδα ασθενών, αποτελεί η IL-13 που επίσης παράγεται από τα Th2 T λεμφοκύτταρα.
Ο ρόλος των Th17 στη σαρκοείδωση παραμένει αδιευκρίνιστος. Έχει αναφερθεί από ορισμένους συγγραφείς
ότι, εκτός από την Th1 πόλωση, τα CD4+ κύτταρα του βρογχοκυψελιδικού εκπλύματος
παρουσίαζαν
χαρακτηριστικά συμβατά με Th17 πόλωση και πιθανόν τα Th17 Τ κύτταρα συμμετέχουν στο σχηματισμό
κοκκιωμάτων. Αντίθετα
σε άλλη εργασία βρέθηκε μειωμένη έκφραση του mRNA της IL-17A στα CD4+ βρογχοκυψελιδικά κύτταρα σε πάσχοντες από
σαρκοείδωση σε σχέση με φυφυσιολογικούς μάρτυρες. Γενικά όλα τα ως σήμερα γνωστά
εργαστηριακά ευρήματα ενισχύουν την άποψη ότι η σαρκοείδωση είναι νόσημα που
χαρακτηρίζεται κατά κύριο λόγο από Th1 πόλωση.
Επί πλέον οι
κλινικές παρατηρήσεις ενισχύουν την άποψη ότι η Th1 πόλωση είναι τυπικό και παθογενετικό γνώρισμα
της σαρκοείδωσης. Η θεραπευτική χρήση
βιολογικών παραγόντων που ενισχύουν την Th1 απόκριση, όπως οι IFN-α, IFN-γ και IL-2 σχετίζεται με αυξημένη επίπτωση πρωτοεμφανιζόμενης ή
υποτροπιάζουσας σαρκοείδωσης. Το ίδιο
έχει παρατηρηθεί με την αποκατάσταση της ανοσίας μετά από χορήγηση εντατικής
αντιρετροϊκής θεραπείας (HAART). Τέλος η
συσχέτιση της σαρκοείδωσης με την 5q-μυελοδυσπλασία με εξάλειψη γονιδίων που
κωδικοποιούν Th2 κυτταροκίνες, όπως η IL-4, ενισχύουν τη σημασία της Th1 πόλωσης στην παθογένεια της σαρκοείδωσης.
Ρόλος του TNF
Ο παράγων
νέκρωσης όγκων (TNF) έίναι γνωστός μεσολαβητής σχηματισμού
κοκκιωμάτων. Κύτταρα από πνεύμονα
ασθενών με σοβαρή ή προϊούσα σαρκοείδωση απελευθερώνουν ex vivo μεγαλύτερες ποσότητες TNF σε σχέση με ασθενείς στους οποίους η νόσοςείναι
ανενεργός. Θεραπεία με αναστολείς του
TNF σε πάσχοντες από σαρκοείδωση είχε ως αποτέλεσμα
βελτίωση της πνευμονικής λειτουργίας και υποχώρηση των εξωπνευμονικών
εκδηλώσεων, γεγονός που τεκμηριώνει τη σημασία αυτής της κυτταροκίνης στην
παθογένεια της νόσου. Αντίθετα άλλες
προφλεγμονώδεις κυτταροκίνες, όπως η IL-1, o MIF και η IL-6, αν και υπερεκκρίνονται, δεν έχουν ξεκάθαρα
ενοχοποιηθεί στην παθογένεια της σαρκοείδωσης.
Παράλληλα με
την υπερέκκριση προφλεγμονωδών κυτταροκινών σε πάσχοντες από σαρκοείδωση
παρατηρείται υπερπαραγωγή από τα κύτταρα του πνεύμονα μεταγραφικών παραγόντων
της οικογένειας NFκΒ.
Αντίθετα υπάρχει ελαττωμένη παραγωγή του αντιφλεγμονώδους μεταγραφικού
παράγοντα PPAR-γ.
Ανοσορρυθμιστικά κύτταρα
Τα Τ
ρυθμιστικά κύτταρα (Treg) περιορίζουν την άνοση απόκριση καταστέλλοντας
τη λειτουργία τόσο των υπεύθυνων παρουσίασης αντιγόνου κυττάρων όσο και των
τελικών Effector T κυττάρων.
Μια ομάδα αυτών των φυσικά υπαρχόντων κυττάρων είναι FoxP3 θετικά καταστέλλουν την παραγωγή προφλεγμονωδών
κυτταροκινών και αναστέλλουν το σχηματισμό κοκκιωμάτων in
vitro.
(να βάλω βιβλιογραφια ιδεα μεδικαλ νιουσλεττερ)
Σε ασθενείς με σαρκοείδωση βρέθηκε ότι είναι
ελαττωμένος ο αριθμός των FoXP3+ Treg κυττάρων αλλά και η έκφραση του FoXP3 των Τ κυττάρων ειδικά αυτών που απομονώνονται
σε υλικό από πνεύμονα. Τα
ευρήματα αυτά συνηγορούν στην άποψη ότι η σαρκοείδωση συνοδεύεται από
ανεπάρκεια της φυσικής ανοσορρυθμιστικής λειτουργίας, αλλά εξακολουθεί να
παραμένει αβέβαιο αν αυτή η ανεπάρκεια παίζει σημαντικό ρόλο στην εμφάνιση
της σαρκοειδικής φλεγμονής.
Το
αγγειοδραστικό εντερικό πεπτίδιο (VIP) είναι μια πεπτιδική ορμόνη με γνωστή
ανοσορρυθμιστική δράση στις χρόνιες φλεγμονές. Η χορήγηση εισπνοών VIP σε ασθενείς με σαρκοείδωση οδήγησε σε βαθμιαία αύξηση
του αριθμού των CD4+CD127-CD25+ Treg κυττάρων και σε ελάττωση της παραγωγής TNF από τα κύτταρα του πνεύμονα. Εξ άλλου πειραματικές μελέτες απέδειξαν
την ιδιότητα του VIP να μετατρέπει in vitro τα άωρα CD4+CD25- T κύτταρα σε CD4+CD25+FoxP3+ Treg κύτταρα.
Οι μελέτες αυτές οδήγησαν τους Prasse et al να προτείνουν την εισπνοή VIP ως μέθοδο θεραπείας πνευμονικών νοσημάτων
ανοσολογικής αιτιολογίας μεταξύ των οποίων και της σαρκοείδωσης.
Σε μια ομάδα
ασθενών με σαρκοείδωση χωρίς σύνδρομο Löfgen βρέθηκε ελαττωμένος αριθμός NK T κυττάρων στο αίμα, τους λεμφαδένες και τον
πνευμονικό ιστό. Το αποτέλεσμα
οδήγησε τους συγγραφείς να διατυπώσουν την άποψη ότι η ανεπάρκεια ΝΚ Τ
κυττάρων συμβάλλει στην εμφάνιση χρόνιας ενεργού φυματίωσης.
Συμφυής ανοσία
Ο ρόλος της
συμφυούς ανοσίας στην παθογένεια της σαρκοείδωσης έχει ελάχιστα μελετηθεί με εξαίρεση την ούτως καλούμενη
κατάσταση πρώτης απόκρισης (first-responder status) της συμφυούς
άνοσης απόκρισης στην κάκωση ή τη λοίμωξη και τη λειτουργία της ρύθμισης της προσαρμοζόμενης
ανοσίας. Υπάρχει η άποψη πως τα
δενδριτικά κύτταρα παίζουν κεντρικό ρόλο στην παθογένεια της σαρκοείδωσης
αλλά τα υπάρχοντα στοιχεία που στηρίζουν αυτή την ιδέα είναι περιορισμένα. Υπάρχουν αρκετές μελέτες που δείχνουν πως οι
υποδοχείς TLR εμπλέκονται στη ρύθμιση της συμφυούς άνοσης
απόκρισης σε ασθενείς με σαρκοείδωση.
Σε μια μελέτη βρέθηκε πως ο πολυμορφισμός των TLR2 συνδέεται με αυξημένη έκφραση των
προφλεγμονωδών κυτταροκινών TNF, IL-12 και IL-6 στα μονοκύτταρα του αίματος ασθενών με
σαρκοείδωση. Σε άλλη
εργασία οι συγγραφείς του άρθρου βρήκαν ότι η διέγερση των TLR2 με αμυλοειδές Α του ορού (SAA) προάγει την παραγωγή TNF.
Αν και αρκετές μελέτες δείχνουν πως η συμφυής
άνοση απόκριση έχει κρίσιμη θέση στην ανοσοπαθογένεια της σαρκοείδωσης, οι
μηχανισμοί δεν έχουν σαφώς διευκρινιστεί.
Μηχανισμοί της ίνωσης
Το δυσάρεστο κλινικό αποτέλεσμα της
κοκκιωματώδους φλεγμονής στη σαρκοείδωση είναι ότι καταλήγει σε ίνωση του πνεύμονα, της καρδιάς
και του ήπατος. Οι μηχανισμοί που
συμβάλλουν στην ινωτική κατάληξη δεν είναι, αν μάλιστα
λάβουμε υπόψη πως η IFN-γ που απελευθερώνεται στα σημεία της
κοκκιωματώδους φλεγμονής, δρα ανασταλτικά στον πολλαπλασιασμό των ινοβλαστών
και την εναπόθεση διάμεσης θεμέλιας ουσίας (κολλαγόνου). Αντίθετα
άλλες κυτταροκίνες όπως οι TGF-β, IGF-1 και μεταλλοπρωτεϊνάσες που εκκρίνονται στα
σημεία σαρκοειδικής φλεγμονής επάγουν την ινωτική διεργασία. Υπάρχουν
ενδείξεις πως σε ασθενείς με ίνωση από
σαρκοείδωση τα
κυψελιδικά μακροφάγα εκφράζουν ένα εναλλακτικό Μ2 φαινότυπο που
χαρακτηρίζεται από αυξημένη έκκριση χημειοκινών, όπως η CCL-18, που προάγει την αναδιαμόρφωση των αεραγωγών
ευνοώντας την ίνωση (εδώ να βάλω
βιβλιογραφία από το ιδεα μεδικαλ).
Με δεδομένο την έλλειψη Th2 κυττάρων που εκφράζουν την IL-4, έχει διατυπωθεί η
άποψη ότι ίσως οι ιντερλευκίνες IL-10 και IL-13 προάγουν τη διαφοροποίηση των μακροφάγων σε προϊνωτικό φαινότυπο.
Είναι φανερό
ότι πρέπει να εντατικοποιηθεί η έρευνα όσον αφορά στους σημαντικούς μηχανισμούς ίνωσης στη
σαρκοείδωση ώστε να
προληφθεί η τελική ίνωση.
Summary
Immunology of sarcoidosiAnaphylaxis and other side effects of omalizumabs. Anthony Papaconstantinou
Omalizumab is
a monoclonal anti-IgE antibody used to treat allergic asthma and chronic
urticaria. In this review we refer to the adverse effects of
the drug with an emphasis on anaphylaxis which is a life-threatening
condition. Other side effects of omalizumab include a potential
effect on malignancy,
risk of parasite disease, and immunological effects including
serum sickness and
Churg-Strauss syndrome.Sarcoidosis
is a multisystem inflammatory disease characterized by noncaseating granulomas.
----- The disease most commonly affects
the lungs, lymph nodes, eyes and skin.
Immunologic
hallmarks of the disease include highly
polarized expression of cytokines produced by Th1 cells and TNF at sites of inflammation. By contrast cytokines released by Th2
cells are downregulated. The role of
Treg cells as well as innate immune mechanisms
remains uncertain. Finally, mMore research effort is necessary to define the
mechanisms of fibrosis in sarcoidosisa.
Περίληψη
Η σαρκοείδωση
είναι πολυσυστηματική φλεγμονώδης νόσος, που χαρακτηρίζεται από σχηματισμό κοκκιωμάτων
χωρίς κεντρική τυροειδοποίηση. Η
νόσος προσβάλλει συχνότερα τους πνεύμονες, τους λεμφαδένες, τους οφθαλμούς
και το δέρμα. Στα ιδιαίτερα
ανοσολογικά χαρακτηριστικά της νόσου περιλαμβάνεται η έντονη πόλωση στην
παραγωγή κυτταροκινών των Th1 κυττάρων
και TNF στα σημεία της φλεγμονής.
Αντίθετα είναι μειωμένες οι κυτταροκίνες που απελευθερώνονται από τα
Th2
Βιβλιογραφία
Busse W, Buhl R, Fernandez Vidaurre C, Blogg M, Zhu
J, Eisner MD, Canvin J. Omalizumab and the risk of malignancy: results from a
pooled analysis. J Allergy Clin
Immunol. 2012; 129(4):983-9.e6.
[PubMed]
Cox L,
Platts-Mills TA, Finegold I et al., American Academy of Allergy, Asthma & Immunology.
American College of Allergy, Asthma and Immunology. American Academy of
Allergy, Asthma & Immunology/American College of Allergy, Asthma and
Immunology Joint Task Force Report on omalizumab-associated anaphylaxis. J Allergy Clin
Immunol. 2007, 120(6):1373-7.
[PubMed]
Kumar C, Zito
PM. (Last
Update: August 25, 2022). Omalizumab.
Treasure Island (FL): StatPearls Publishing.
Retrieved June 11, 2023
Plosker GL,
Keam SJ. . Omalizumab: a
review of its use in the treatment of allergic asthma. BioDrugs.
2008;22(3):189-204.
Tong P,
Wessermann DR. Molecular
Mechanisms of IgE Class Switch Recombination. Current Topics
in Microbiology and Immunology, 2015, 388: 21-37. doi:
10.1007/978-3-319-13725-4 2 (Full text).
Van de Kamer JH, ten Bokkel
Huinink H, Weijers HA. Rapid
method for the determination of fat in feces. J Biol Chem. 1949, 177:347-355.
Walters MP, Kelleher J, Gilbert J, Littlewood JM.
Clinical monitoring of steatorrhea in cystic fibrosis. Arch Dis Child 1990, 65:99-102 (Full text)
► Επιστροφή στην
πρώτη σελίδα του IDEA Medical Newsletter
|

